Exercício resolvido de Física. Questão que exige conhecimentos de termologia: gases perfeitos, equação geral dos gases.
(Gases – 03) Na figura, encontramos esquematizados dois recipientes conectados e separados por uma válvula, inicialmente fechada. Um mesmo gás ideal ocupa ambos os recipientes, conforme a indicação. Se abrirmos a válvula, a que temperatura deve ser elevada a mistura para que no final tenhamos uma pressão de 10 atm?
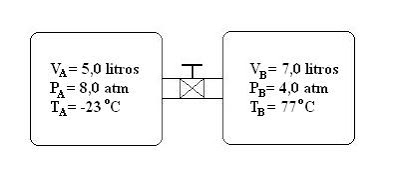
Resolução
Antes de iniciar a resolução devemos lembrar que a temperatura deve ser sempre utilizada na escala Kelvin, para as conversões utilizamos a seguinte equação: K = C + 273
K = C + 273
K = -23 + 273 = 250K
K = C + 273
K = 77 + 273 = 350K
Agora podemos continuar utilizando a equação dos gases.
 K = C + 273
K = C + 273500 = C + 273
C = 500 – 273
C = 227 °C
Resposta:
A temperatura que deve ser elevada a mistura para que no final tenhamos uma pressão de 10 atm é igual a 227 °C.
O mesmo exercício pode ser resolvido de outra maneira.
Voltar para os Exercícios Resolvidos de Física
Eu fiz assim de primeira e deu certinho 😉 Obrigado pelo exercício, muito bom!
Daonde surgiu aquele V=12
Daonde surgiu aquele V=12
Pois ela somou o volume dos dois recipientes 5+7
Tenho dúvidas sobre a velocidade média das moléculas de um gás perfeito e não estou encontrando exercícios resolvidos referente ao assunto, gostaria de saber se vocês podem disponibilizar algum material sobre tal.